15.8. Trong ngành công nghệ lọc hóa dầu, các ankan thường được loại bỏ hydrogen trong các phản ứng dehydro hóa để tạo ra những sản phẩm hydrocarbon không no có nhiều ứng dụng trong công nghiệp. Hãy tính biến thiên enthalpy chuẩn của các phản ứng sau dựa vào năng lượng liên kết. (Giá trị một số năng lượng liên kết được cho trong Phụ lục 2, SGK Hóa học 10, Cánh Diều)
a) H3C – CH2 – CH2 – CH3 → CH2 = CH – CH = CH2 + 2H2
b) 6CH4 → C6H6 (1,3,5 – cyclohexatriene) + 9H2
Cho biết công thức cấu tạo của 1,3,5 – cyclohexatriene như sau:
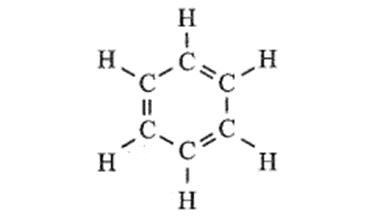
Các phản ứng trên có thuận lợi về phương diện nhiệt hay không? Phản ứng theo chiều ngược lại có biến thiên enthalpy bằng bao nhiêu?
Bài Làm:
a) PTHH: H3C – CH2 – CH2 – CH3 → CH2 = CH – CH = CH2 + 2H2
$ \Delta _{r}H_{298}^{o}$ =(10EC−H+3EC−C)−(6EC−H+2EC=C+EC−C)−2EH−H
=10×414 + 3×347 − (6×414 + 2×611 + 347) − 2×436=256(kJ) < 0.
b) PTHH: 6CH4 → C6H6 + 9H2
$ \Delta _{r}H_{298}^{o}$ =6×4EC−H−(6EC−H+3EC=C+3EC−C)−9EH−H
=24×414 − (6×414 + 3×611 + 3×347) - 9×436=654(kJ) < 0.
Các phản ứng này là phản ứng thu nhiệt nên không thuận lợi về phương diện nhiệt.
Phản ứng theo chiều ngược lại thuận lợi về phương diện nhiệt:
CH2 = CH – CH = CH2 + 2H2→ H3C – CH2 – CH2 – CH3 $ \Delta _{r}H_{298}^{o}$ = - 256 kJ
C6H6 + 9H2 → 6CH4 $ \Delta _{r}H_{298}^{o}$ = - 654 kJ
